肝脏由许多六边形的肝小叶构成,组织学上用E-钙粘着蛋白划定其区域。由于单向血流,肝脏中存在氧气、营养素和激素的梯度,而一些关键酶(如谷氨酰胺合成酶)的区间分布也提高了代谢效率。研究表明,肝脏枯否细胞富集于门脉系统附近。那么,肝脏的免疫系统是否也存在这种区间分布呢?这种分布方式是否对机体免疫系统存在影响呢?
2020年11月25日《Nature》杂志在线发表了美国国立卫生研究院Ronald N. Germain、Anita Gola等研究人员名为“Commensal-driven immune zonation of the liver promotes host defence”的研究成果。该研究发现,共生细菌驱动肝脏免疫分区并优化宿主免疫功能。

研究人员通过发育分析发现,断奶时枯否细胞在肝脏的肝周区域周围富集,但无菌小鼠的肝脏中不存在这种分区现象。
这种分布是否是断奶期间生理变化导致的呢?研究人员将成年的无菌小鼠与成年的无特定病原体(SPF)小鼠共同喂养后,成年无菌小鼠也出现了枯否细胞的分区。而使用抗生素对SPF小鼠进行处理后,其枯否细胞的门静脉周富集消失。
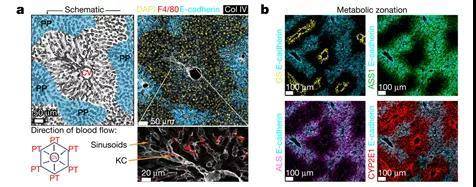
断奶对小鼠肝脏枯否细胞分布的影响
研究人员应用荧光染色,遗传扰动,转录组学等方法和数学建模来重新评估免疫细胞在肝脏中的定位与宿主保护之间的关系。他们发现髓样和淋巴样驻留免疫细胞集中在周围的区域。
这种免疫分区不受发育控制,而是由共生细菌在肝窦内皮细胞中诱导的持续MYD88依赖性信号传导引起的,该信号进而调节参与趋化因子梯度形成的细胞周围基质的组成。

REX3小鼠CXCL9的代表性概率密度图
其后,研究人员评估了免疫肝脏分区对宿主的功能益处。体内实验和建模表明,这种免疫空间极化在防止系统性细菌传播方面比均匀分布更有效。
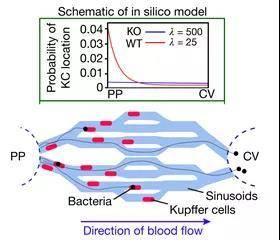
细菌捕获模型示意图
总之,这些数据表明,肝窦内皮细胞可感知微生物组,主动协调免疫细胞的定位,从而优化宿主防御能力。
转载自健康界:https://www.sohu.com/a/436179316_139908